学术前沿

走近我们

母乳成分研究

婴幼儿营养健康

儿童营养健康

孕产妇营养健康

实用工具


撰稿人:李依璇
目前有研究表明乳铁蛋白与骨桥蛋白对婴幼儿肠道屏障功能以及免疫功能具有调节作用。作为在初乳中高丰度存在的蛋白质,乳铁蛋白与骨桥蛋白是否存在协同作用缺乏进一步确认。伊利联合中国农业大学李依璇团队,首次报道了人初乳中高丰度的乳铁蛋白与骨桥蛋白对于保护肠屏障功能以及调节免疫功能的协同作用。
研究成果分别在2023年10月发表于影响因子8.2的国际学术期刊《International Journal of Biological Macromolecules》,以及在2023年12月发表于影响因子为6.1的国际top学术期刊《Food & Function》。
研究主要发现
1. 乳铁蛋白(LF)与骨桥蛋白(OPN)和联合作用时,能够减少LPS诱导下的肠道通透性增加,保护肠道屏障完整性;
2. LF与OPN联合使用改变了肠道干细胞的分化方向;
3. LF与OPN联合使用抑制LPS诱导的肠道固有层的炎症反应。
研究背景
婴幼儿肠道发育不完善,外界环境容易使肠道屏障受损,肠道屏障的受损增加了炎症性肠病(IBD)的风险,这对公共卫生造成了重大负担。虽然已经制定了一些IBD治疗策略,但它们具有不良影响。一些研究表明,针对革兰氏阴性菌的抗生素可诱导血液和肠道内LPS水平急剧升高;并且广谱抗生素的长期和广泛使用引起肠道生态失调,削弱肠道的生物屏障功能,并进一步破坏上皮屏障,进而引起更严重的肠道疾病,如坏死性小肠结肠炎、溃疡性结肠炎等。母乳中存在大量的功能因子,对婴幼儿肠道健康不可或缺,但由于不同地区、年龄、个人因素、营养状态等因素的影响,导致很多母亲无法纯母乳喂养婴儿,因此婴幼儿配方奶粉的发展越发迅速。母乳是个复杂的系统,单一成分的功能已无法满足婴幼儿对营养的需求,因此解释母乳中活性成分之间的协同作用对婴配粉的更新换代起到至关重要的作用。
乳铁蛋白(LF)与骨桥蛋白(OPN),在人类初乳高丰度存在,并随着泌乳期的延长,含量逐渐降低,被认为与早期肠道发育有关,增强肠道功能;但尚未有研究表明两种功能蛋白之间在体内展现出协同作用,因此探究两种蛋白在体内是否具有协同作用关系,对于婴幼儿配方奶粉母乳化以及婴幼儿肠道健康的保护至关重要。
研究方法
本研究采用预防模型,给予4周龄小鼠灌胃乳铁蛋白、骨桥蛋白以及两种蛋白不同比例的混合蛋白,干预一周后,评估蛋白联合组是否缓解LPS引起肠道功能的损伤,实验流程图如下(图1):
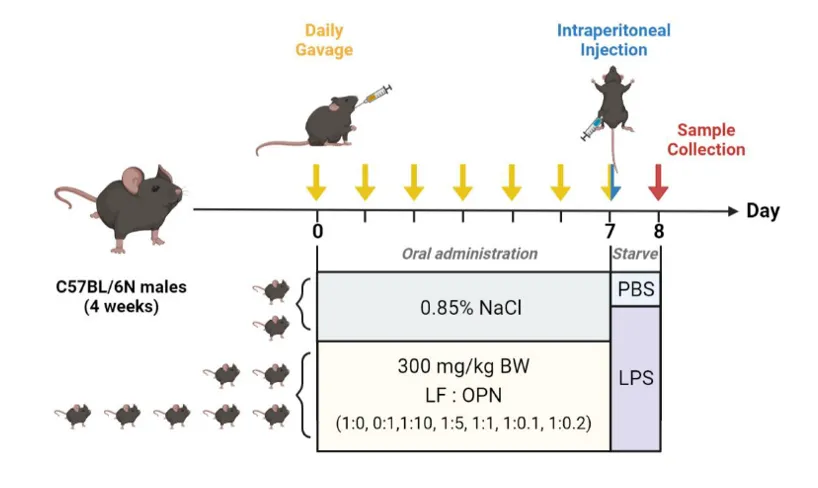
图1: 实验流程图
研究结果
01. LF和OPN对动物体重的变化以及肠道通透性的影响
研究记录了整个实验流程中动物体重的变化,各组之间均没有显著差异;通过测量血清中二胺氧化酶(DAO)活性以及D-乳酸含量以及体外测量空肠的通透性(FITC)表明肠屏障的损伤程度,结果如图2所示,发现模型组的DAO活性、D-乳酸含量以及FITC含量均显著高于对照组,并发现当LF:OPN=1:5时发挥的功能效果优于单独的LF与OPN,接下来探究LF:OPN=1:5(LOP)与单独LF、OPN是否具有协同作用。
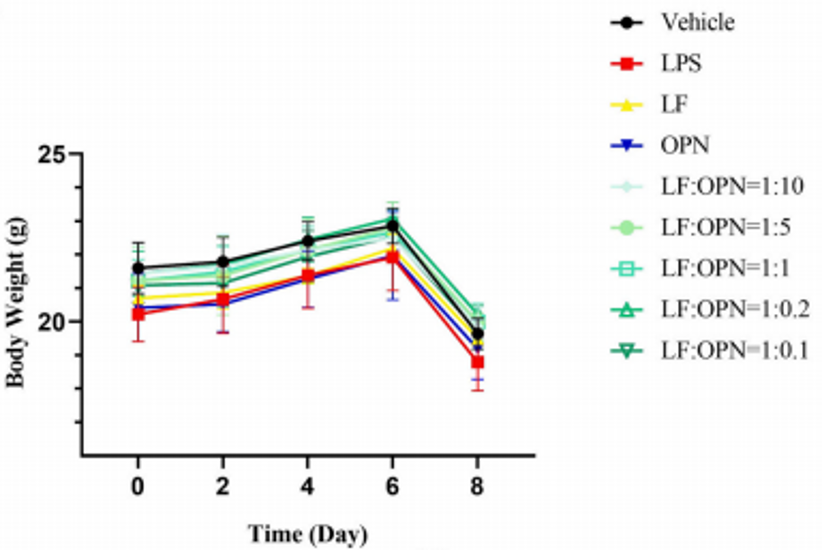
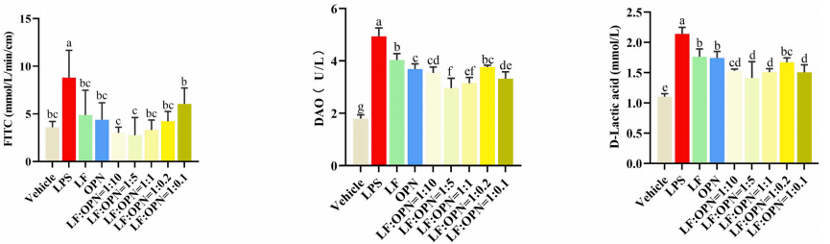
图2: 动物体重变化与肠道通透性变化
01.LF联合OPN减轻LPS诱导的肠道炎症反应
为了确定LF与OPN在免疫调节功能上是否有协同效应,检测了血清中免疫因子的含量,结果如图3所示,与对照组相比,LPS组血清促炎因子肿瘤坏死因子-α(TNF-α)、白细胞介素6(IL-6)和白细胞介素1β(IL-1β)水平分别显著升高,而血清中抗炎细胞因子,如IL-4和IL-10的水平在LPS处理下显著下降。然而,LF和OPN抑制了这些变化,且两种蛋白联合使用时对炎症反应的响应能力最强。
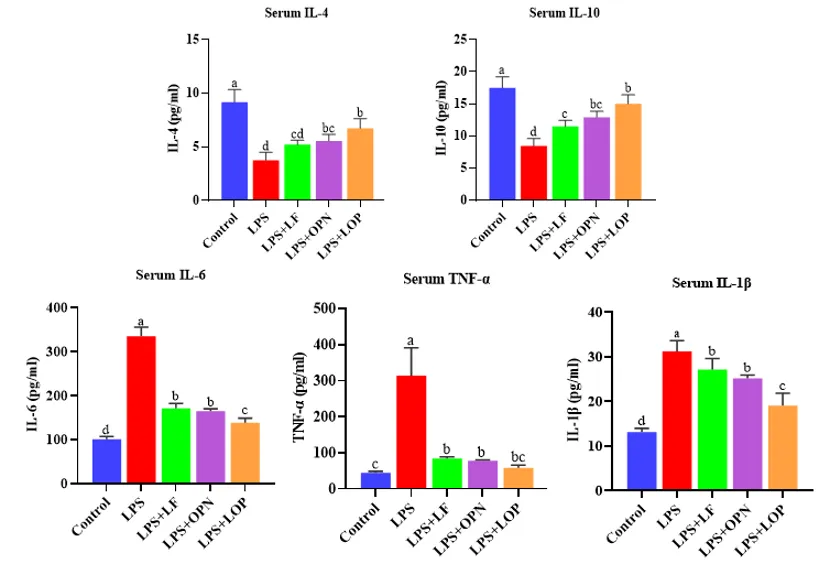
图3: LF联合OPN对LPS诱导小鼠炎症的影响
03. LF联合OPN缓解由LPS引起的肠道炎症
为了探讨LF联合OPN作用是否也能保护肠道免受感染,分析了肠道固有层中的免疫细胞以及他们分泌的免疫因子。通过免疫染色对免疫细胞表面的特征标志物进行定位,结果如图4 A-D所示,在促炎因子诱导下分化为Treg细胞的CD8+ T淋巴细胞在LPS处理后在肠道中数量显著减少,LOP具有上调CD8+ T细胞数量的趋势;中性粒细胞、CD4+ T淋巴细胞、巨噬细胞等免疫细胞在LPS刺激下被激活,与对照组相比,LPS组显著增加这些细胞活化后的数量,LF、OPN和LOP均能降低活化免疫细胞数量的变化,且LOP表现出更强的免疫调节作用。
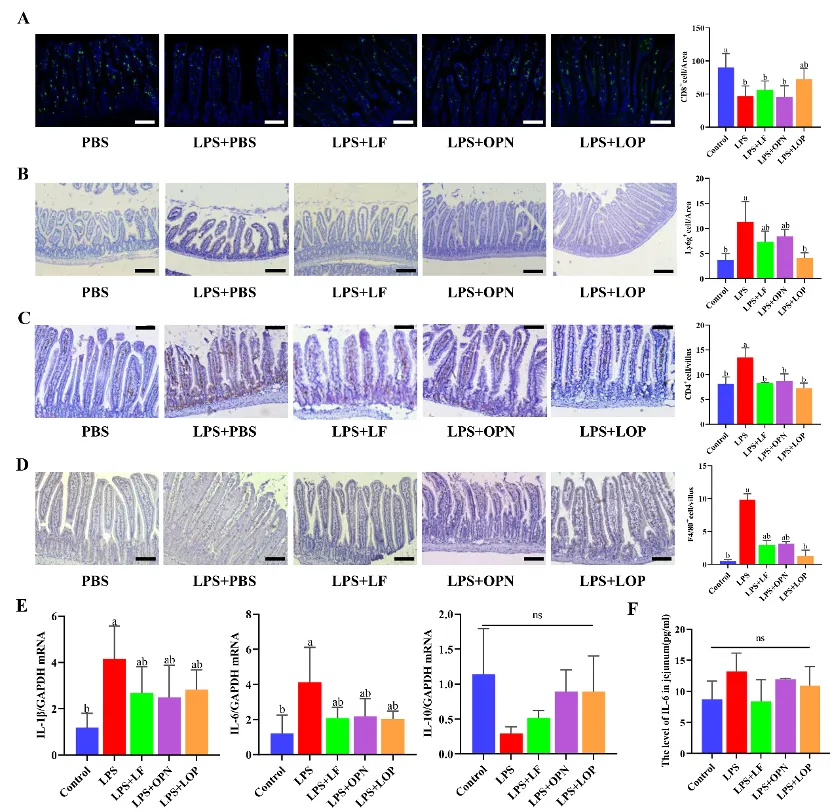
图4: LF联合OPN对LPS诱导下肠道炎症的影响
04. LF联合OPN对LPS诱导下的小肠上皮结构的影响
为了评价LF与OPN对LPS诱导的肠道损伤条件下小肠上皮结构的影响,通过苏木精-伊红染色(HE染色)并对HE评分、绒毛高度、隐窝深度以及绒毛高度与隐窝深度的比值进行统计分析,结果如图5所示,与对照组相比,模型组显著增加了HE评分,显著下调了小肠的绒毛高度与隐窝深度,说明模型建立成功;与模型组、LF+LPS组以及OPN+LPS组相比,LOP+LPS组能够上调绒毛高度,并显著上调隐窝深度,展示出协同作用。
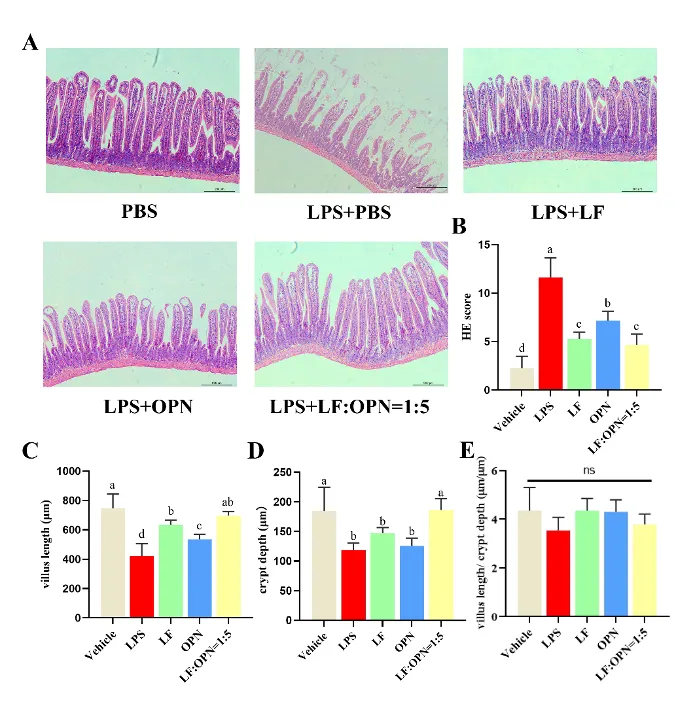
图5: LF与OPN对小肠上皮结构的影响
05. LF联合OPN对LPS诱导下肠道紧密连接的影响
为了分析LF与OPN对LPS诱导下肠道紧密连接的影响,通过扫描电镜、实时荧光定量PCR以及蛋白免疫印迹分析对紧密连接蛋白的功能以及表达量进行评价,结果如图6所示,发现LOP+LPS组与模型组以及单独蛋白组相比,具有更紧凑与整齐的微绒毛结构,并且增加了紧密连接蛋白的表达。
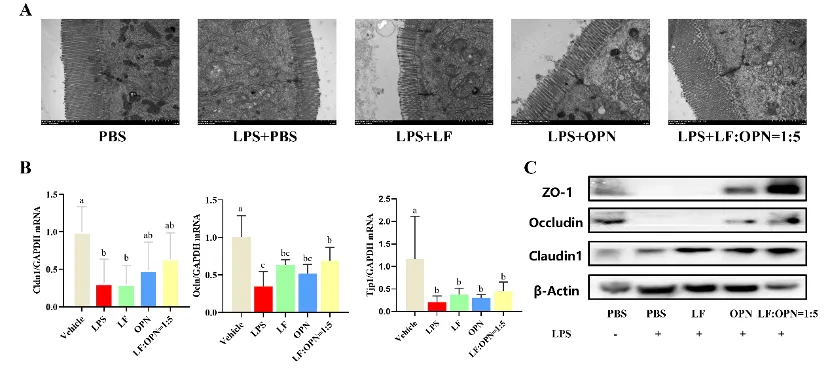
图6: LF与OPN对LPS诱导下肠道紧密连接结构的影响
06. LF联合OPN对LPS诱导下肠道成熟上皮细胞的影响
为了对肠上皮结构中的成熟上皮细胞种类进行分析,通过糖原染色以及免疫荧光染色对吸收细胞以及分泌细胞的标志物进行标记,结果如图7所示,发现与对照组相比,模型组中吸收细胞数量与分泌细胞数量显著下降;与对照组相比,模型组显著下降绒毛中吸收细胞的比例,LOP+LPS组能够显著增加绒毛中吸收细胞所占比例,展现出协同效应。
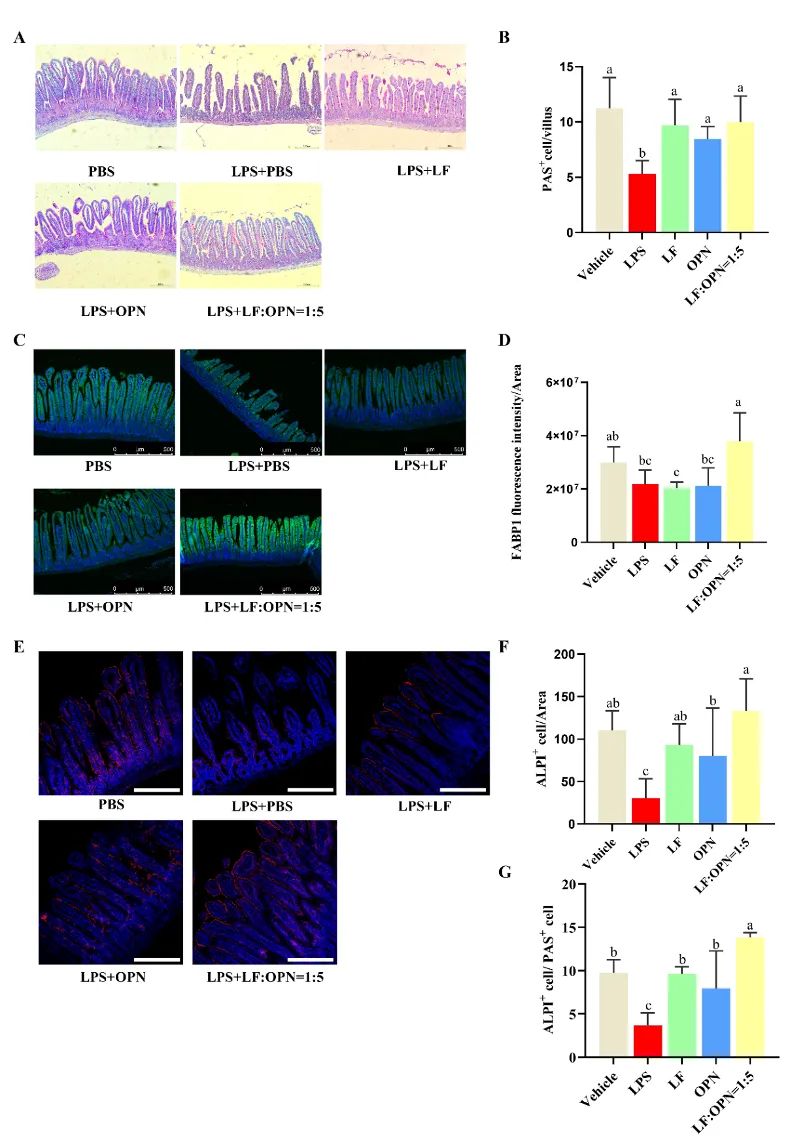
图7: LF与OPN对LPS诱导下肠道成熟上皮细胞组成的影响
07. LF联合OPN对LPS诱导下肠道干细胞功能的影响
为了判断LF与OPN对肠道成熟上皮细胞的来源的影响,通过免疫染色以及TUNEL染色对肠道干细胞功能进行评价,结果如图8所示,与对照组相比,模型组中干细胞数量、增殖能力显著下降,凋亡细胞数量显著增加;与单独蛋白相比,LOP+LPS组显著增加了干细胞增殖能力,但对干细胞数量以及凋亡细胞数量没有显著影响。
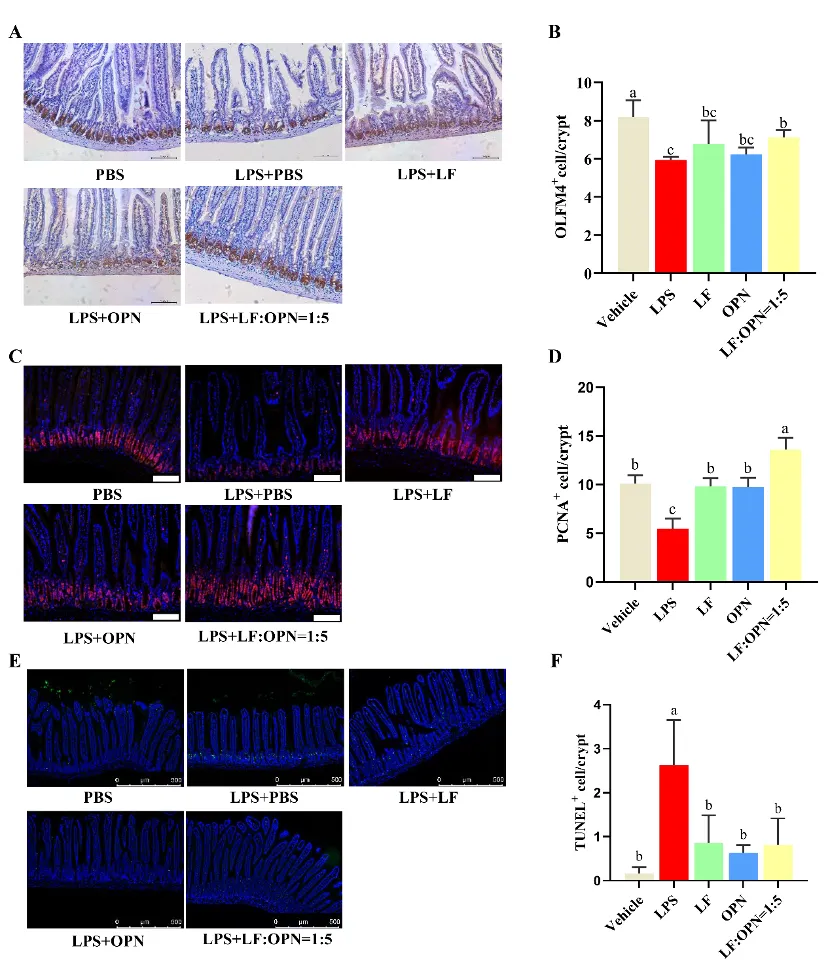
图8: LF与OPN对LPS诱导下肠道干细胞功能的影响
08. LF联合OPN对LPS诱导下Notch通路的影响
为了确定LOP如何影响肠道干细胞命运,通过免疫组化染色以及蛋白免疫印迹分析对调控肠道干细胞分化方向的Notch通路的靶蛋白进行分析,结果如图9所示,模型组显著下调了Hes1在蛋白水平的表达,与其他四个组相比,LOP+LPS组能够显著上调Hes1的表达,从而激活Notch通路。
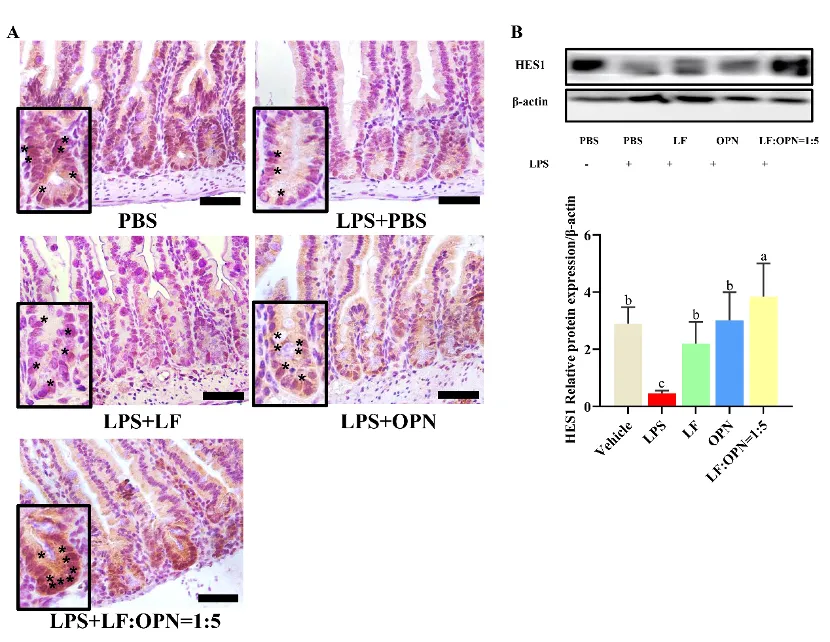
图9: LF与OPN对LPS诱导下肠道干细胞功能的影响
研究结论
研究首次报告了母乳中的乳铁蛋白与骨桥蛋白在体内保护肠屏障以及免调节免疫功能方面的协同作用。研究结果表明,乳铁蛋白与骨桥蛋白联合使用可以激活肠道干细胞的Notch通路,增加肠道干细胞的增殖分化功能,诱导肠道干细胞向吸收型细胞分化,进而增加紧密连接蛋白表达,减少肠屏障损伤情况下的肠道通透性的增加,增强肠屏障功能;并且降低LPS诱导的肠道固有层炎症反应。这些发现可以解释蛋白质之间存在的协同作用,并为婴儿配方奶粉母乳化增添新的依据与证据。
参考文献
[1] C. Li, Y. Sun, T. He, Y. Lu, I. M.-Y. Szeto, S. Duan, Y. Zhang, B. Liu, Y. Zhang, W. Zhang, J. He and Y. Li, Synergistic effect of lactoferrin and osteopontin on intestinal barrier injury, Int. J. Biol. Macromol., 2023, 253, 127416.
[2] Li, C A, Lu Y, Wang J, Liu B, Szeto IMY, Zhang W, Bi R, Duan SF, Quan R, Wang X M, Li Y X, Xiong W, Sun J Z, Sun, Y A. Immunoregulation of bovine lactoferrin together with osteopontin promotes immune system development and maturation. Food Funct., 2024,15, 866-880.