学术前沿

走近我们

母乳成分研究

婴幼儿营养健康

儿童营养健康

孕产妇营养健康

实用工具

新生儿出生时,免疫系统还没有发育完全。摄入母乳后,母乳中的免疫细胞向婴儿转移,对其免疫功能产生影响,促进婴儿免疫系统的发育[1]。
母乳免疫细胞的种类和占比
新鲜母乳含有多种免疫细胞。数据表明,母乳免疫细胞中髓系细胞占据优势,总占比超过80%,其次是淋巴细胞,约占免疫细胞总量的20%。淋巴细胞主要由T细胞组成,约占80%[2]。此外,人类母乳中还发现了自然杀伤(NK)细胞、自然杀伤T细胞(NK-T细胞)、先天淋巴细胞(ILC)、未成熟粒细胞、调节性T细胞(Tregs)等。
值得注意的是,母乳中免疫细胞的组成是动态的,随母乳成熟阶段、母乳喂养期间母体状况而变化[2]。
母乳免疫细胞向婴儿转移过程中所面临的挑战
01、母乳免疫细胞如何在上消化道酸性的条件下存活
上消化道呈强酸性,母乳免疫细胞如何避免受损呢?研究表明,婴儿口腔中的唾液可与母乳发生反应,产生组合代谢物,这种生化过程可保护细胞免受胃酸损伤,帮助母乳免疫细胞存活[3]。此外,婴儿胃中的消化酶和酸度较弱,这种低酸度与母乳的高缓冲能力相结合,可能生产出具有足够高pH值的环境,从而产生了一个母乳免疫细胞存活的机会窗口[4]。
02、母乳免疫细胞通过渗透肠道屏障
肠黏膜会形成物理、生化和免疫屏障,阻止或调节肠腔内容物向间质黏膜下组织转移。婴儿时期,肠黏膜屏障尚未发育完全,使得肠腔中大分子和细胞可以进入婴儿血液,因此当摄入的母乳通过肠腔时,其中的免疫细胞通过肠道屏障的机会增加[5]。
03、母乳免疫细胞如何避免新生儿免疫系统的排斥
母乳免疫细胞之所以能够避免新生儿免疫系统的排斥,是因为“微嵌合”现象的存在。“微嵌合”是一种生物机体中含有来自另一生物机体的少量细胞的现象。这种现象在孕期发生,母亲和胎儿常常交换细胞,而这些细胞能在体内存活数年,母乳喂养同样也会引起微嵌合现象,这种过程被认为会诱导对非遗传母体抗原(NIMA)的耐受性[6]。
母婴免疫系统的相互作用
母乳淋巴细胞来源于母体的肠道相关淋巴组织(GALT)和鼻咽相关淋巴组织(NALT)。母体来源的T淋巴细胞以及分泌IgG的B淋巴细胞进入乳腺,穿过乳腺上皮细胞,进入乳汁(图1A)。此外,婴儿也可能从“肠乳腺途径”获得母体保护,这与在母乳喂养期间逆行导管流动有关,婴儿口腔来源的病原体在吸吮过程中通过乳头转移,以刺激乳房产生局部的免疫反应,分泌特异性免疫球蛋白,然后通过母乳喂养传递给婴儿(图1B)[2]。
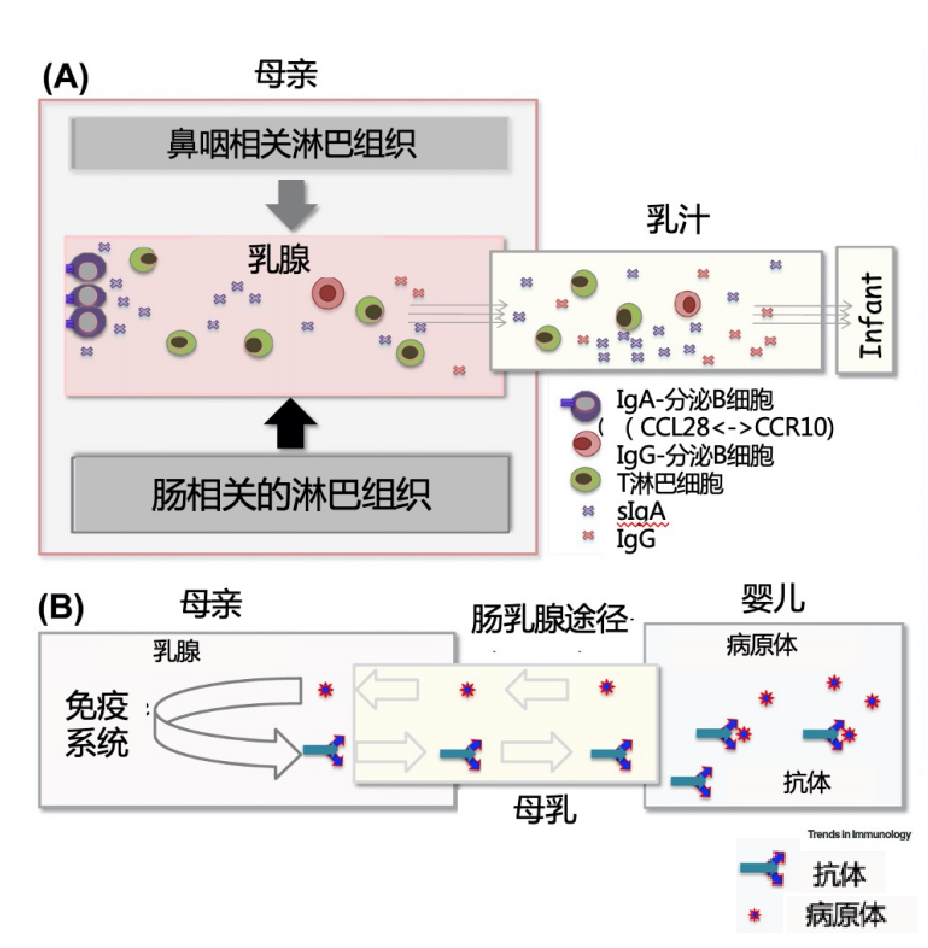
图1.母婴免疫系统的相互作用[2]
母乳免疫细胞在婴儿早期免疫编程中的作用
通过小鼠研究,科学家逐渐发现,母乳喂养过程中,母婴免疫细胞的传递在生命早期免疫编程中发挥作用,逐渐明确母乳免疫细胞对婴儿早期免疫反应、疾病感染和过敏结局都会产生影响。
总体而言,母乳源的免疫细胞,可能影响婴儿T细胞库的发育;同时,支持新生儿免疫防御的肠道免疫并建立体内平衡;此外,母乳源的IgG有助于婴儿建立宿主-微生物共生,保护新生儿免受感染,并对免疫耐受产生影响;而分泌型IgA可通过限制细菌与肠上皮的作用、增强肠道屏障功能、调节肠道菌群等方式发挥免疫作用(详见图2)[2]。
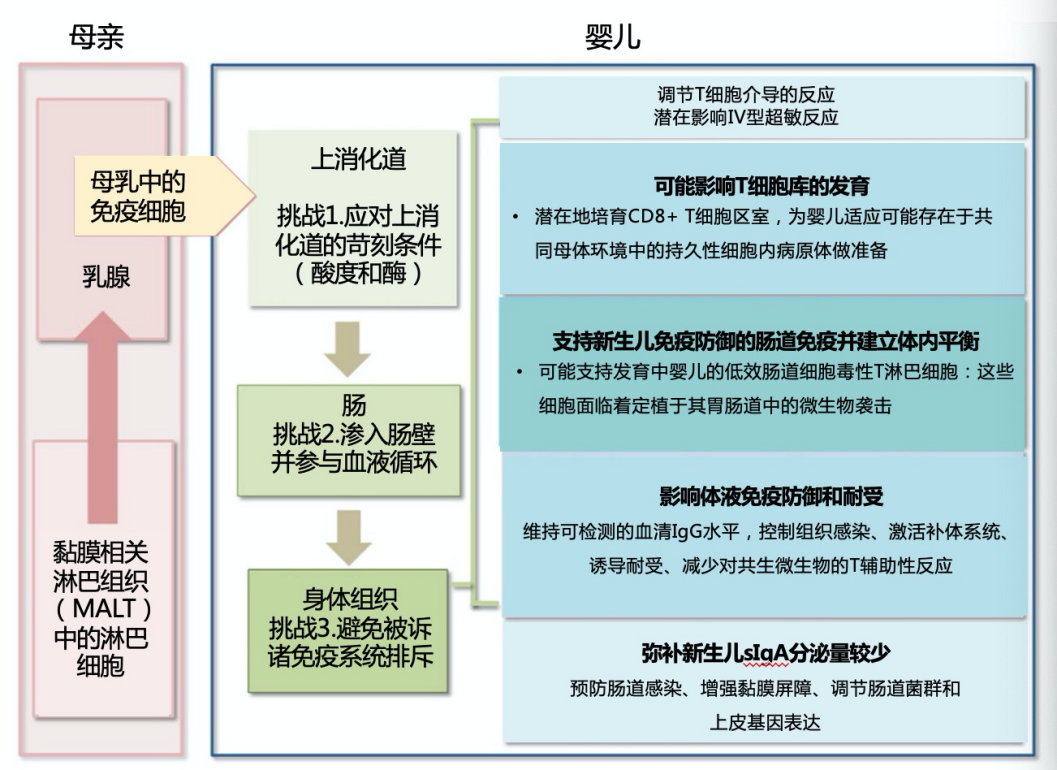
图2.母乳喂养期间母婴细胞免疫转移及其在生命早期免疫编程中的作用[2]
小结和展望
尽管母乳免疫细胞对健康影响的证据在理解深度和研究质量方面不断扩大,但仍然存在许多研究空白。例如:深入了解母体来源的T细胞对正常母乳喂养期间婴儿T细胞库发育的影响;对于母乳细胞以及母体的免疫细胞如何避免被婴儿免疫系统攻击的机制,目前仍知之甚少;此外,与母乳喂养和肠道黏膜保护相关的生命早期免疫机制也值得深究。
最终,阐明母体因素在新生儿免疫编程中的作用和临床结局,为明确可以针对孕期或新生儿干预措施提供基础,以促进婴儿健康。
参考文献:
[1]Camacho-Morales A, Caba M, García-Juárez M, et al. Breastfeeding Contributes to Physiological Immune Programming in the Newborn[J]. Frontiers in Pediatrics, 2021: 1120.
[2]AmaleLaouar. Maternal Leukocytes and Infant Immune Programming During Breastfeeding. Trends Immunol. 2020 Mar;41(3):225-239.
[3]Al-Shehri S S, Knox C L, Liley H G, et al. Breastmilk-saliva interactions boost innate immunity by regulating the oral microbiome in early infancy[J]. PloS one, 2015, 10(9): e0135047.
[4]Cabinian A, Sinsimer D, Tang M, et al. Transfer of maternal immune cells by breastfeeding: maternal cytotoxic T lymphocytes present in breast milk localize in the Peyer’s patches of the nursed infant[J]. PloS one, 2016, 11(6): e0156762.
[5]Saleem B, Okogbule-Wonodi A C, Fasano A, et al. Intestinal barrier maturation in very low birthweight infants: relationship to feeding and antibiotic exposure[J]. The Journal of pediatrics, 2017, 183: 31-36. e1.
[6]Shrivastava S, Naik R, Suryawanshi H, et al. Microchimerism: A new concept[J]. Journal of oral and maxillofacial pathology: JOMFP, 2019, 23(2): 311.