学术前沿

走近我们

母乳成分研究

婴幼儿营养健康

儿童营养健康

孕产妇营养健康

实用工具

母乳营养成分是动态变化的,但母体饮食结构是否会对母乳中的营养成分产生影响,我们仍知之甚少。近期,Scientific Reports发表的一篇关于母体饮食对母乳中低聚糖影响的文献提出了全新的观点,指出特定的母体饮食或可改变母乳HMO的构成,从而达到塑造母乳微生物的作用。
一、研究背景
低聚糖(HMO)是母乳中含量仅次于乳糖和脂肪的第三大成分。HMO作为生物活性大分子,无法在婴儿肠道被消化,但却可作为细菌的底物,与母乳微生物共同参与构建婴儿肠道微生态,在婴儿健康的发展中发挥有益作用。母乳低聚糖的含量和种类受到遗传、环境、胎次等因素的影响,然而尚没有研究能明确母亲的饮食、母乳HMO构成和母乳微生物组之间是否存在因果关系。该研究旨在明确哺乳期间改变母体饮食中的关键成分是否会起到驱动特定HMO分泌的作用,进而塑造母乳微生物组。
二、研究设计
该研究通过交叉试验设计,进行两个单独的单盲交叉饮食干预研究,详细的研究设计方案见图1,所收集的样本通过全基因组测序的方法对母乳微生物组的分类和功能进行分析。
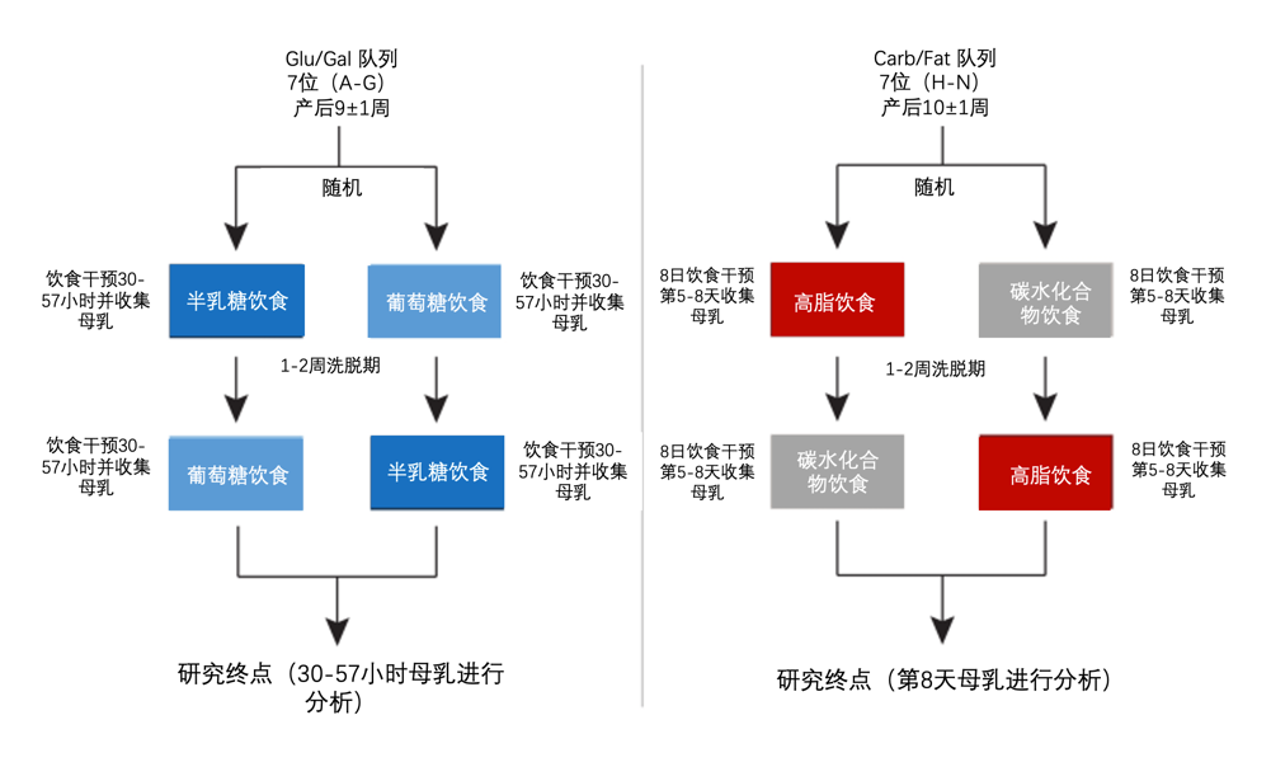
图1. 研究设计
三、研究结果
01 母亲饮食改变母乳中HMO的分布
研究显示,在采集的母乳样本中,70%的HMO为岩藻糖基化HMO和唾液酸化HMO。总体而言,半乳糖和高脂饮食分别使HMO增加50%和30%,而其它饮食HMO则较为稳定。
在Glu/Gal队列中,相对于半乳糖饮食,葡萄糖饮食中岩藻糖基化HMO的浓度降低;在Carb/Fat队列中,与碳水化合物饮食相比,高脂肪饮食中唾液酸化HMO的浓度降低(图2)。
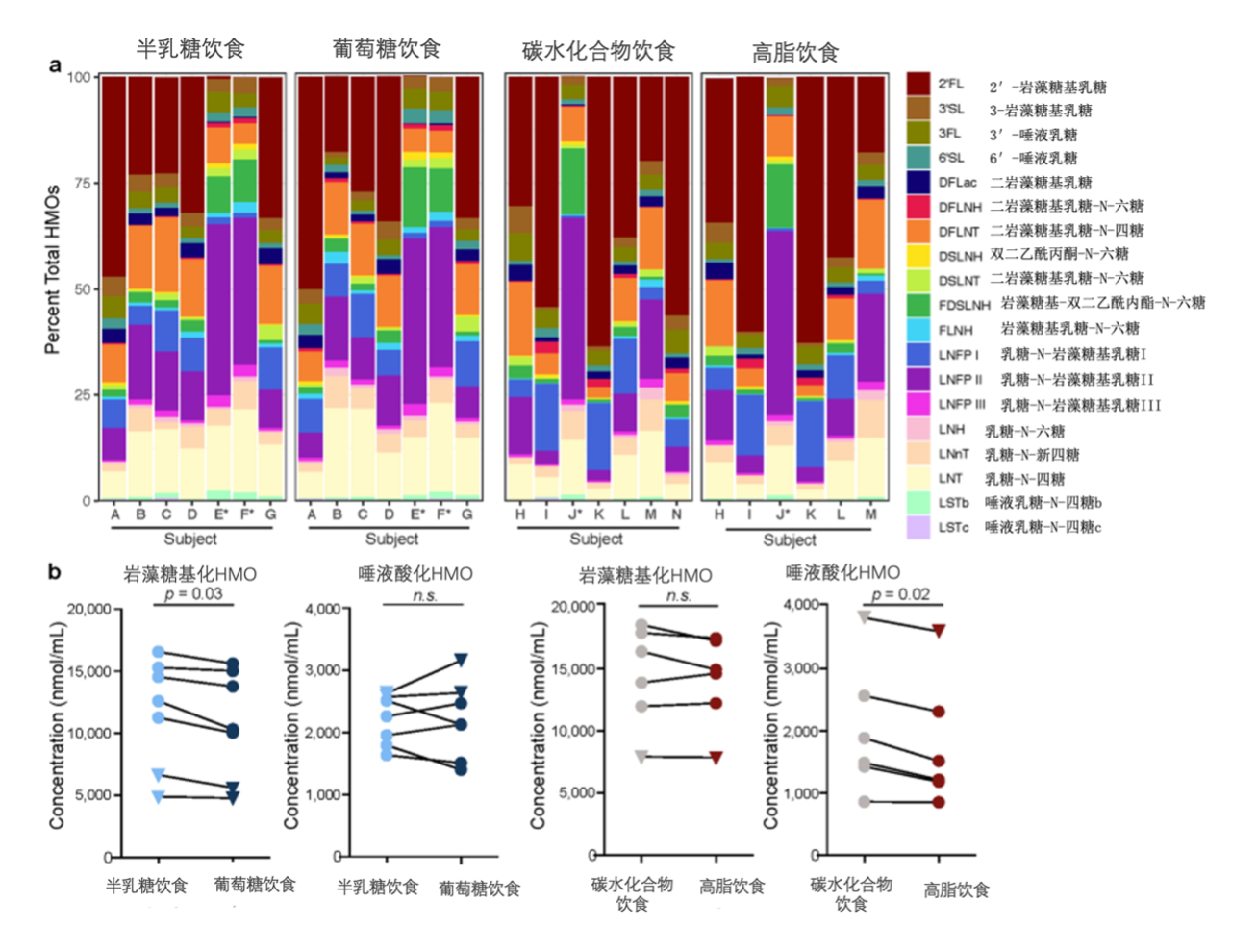 图2.母体饮食对母乳HMO的分布的改变情况
图2.母体饮食对母乳HMO的分布的改变情况
(a) 基于摩尔浓度的每个队列中单个HMO的相对丰度(绿色:岩藻糖基化HMO,紫色:唾液酸化HMO;a–N:受试者标识符;星号:非分泌型)
(b) 与半乳糖饮食相比,葡萄糖饮食后岩藻糖基化HMO显著降低(配对t检验,p = 0.03),唾液酸化HMO无明显变化
(c) 高脂饮食显著降低唾液酸化HMO(配对t检验,p = 0.02),HMO结合岩藻糖无明显变化。
圆:分泌型;三角形:非分泌型
02 母体饮食影响母乳微生物的基因功能和氨基酸代谢

图3.通过WGS测序分析不同饮食母乳微生物宏基因组的差异
(a)葡萄糖与半乳糖饮食线性判别分析(LDA)
(b)高碳水化合物与高脂肪饮食线性判别分析(LDA)
(c)氨基酸生物合成途径的热图,揭示母乳微生物氨基酸的生物合成途径
03 半乳糖饮食、岩藻糖基化HMO与细菌岩藻糖苷酶显著相关
岩藻糖苷酶是细菌分泌的一种能够从糖中去除岩藻糖残基的酶,该研究测定细菌岩藻糖苷酶的基因丰度,并评估其与母乳中岩藻糖基化HMO的关系。岩藻糖苷酶的丰度也与半乳糖饮食有关(图4c),岩藻糖苷酶增加的幅度与样品中岩藻糖基化HMO的增加幅度成正比(图4a、4b),这提示我们,饮食引起的岩藻糖基化HMO增加可能是所观察到的岩藻糖苷酶丰度变化的驱动因素。具有岩藻糖苷酶的细菌物种的相对丰度表明,具有岩藻糖苷菌群的多数是链球菌属(图4e)。

图4. 岩藻糖基化HMO的水平与母乳微生物组中细菌岩藻糖苷酶基因的丰度密切相关
(a)Glu / Gal队列HMO结合的岩藻糖浓度与细菌岩藻糖苷酶丰度线性回归分析(ShortBRED法 R = 0.98,p = 0.003);字母:受试者ID;浅蓝色:半乳糖饮食,深蓝色:葡萄糖饮食
(b)Glu / Gal队列中HMO结合岩藻糖和细菌岩藻糖苷酶丰度的线性回归分析(PICRUSt法R = 0.88,p = 0.0009)
(c)相对于葡萄糖饮食,岩藻糖苷酶丰度随半乳糖增加(p = 0.030,配对t检验)
(d)岩藻糖苷酶丰度的增加幅度与岩藻糖基化HMO的增加成正比(R = 0.88,p = 0.048,线性回归)
(e)Glu / Gal队列样本中,含有岩藻糖苷酶的细菌菌种的相对丰度
四、研究结论
母体饮食中特定碳水化合物和宏量营养元素的摄入会改变母乳中HMO的浓度,而HMO作为细菌代谢的底物,岩藻糖基化HMO浓度与母乳微生物所具有的岩藻糖苷酶的基因丰度之间存在显著关联。母体饮食或可通过对母乳中HMO构成的改变,进而影响母乳微生物生态。
参考文献: